FAQs
Qu'est-ce que le saccharose ?
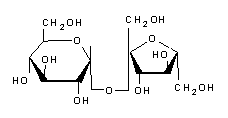
"Le D(+)-saccharose, ou sucre commun, est un disaccharide composé de glucose et de fructose, deux sucres simples ou monosaccharides. La liaison qui unit les deux monosaccharides est de type O-glycosidique, cette liaison est dicarbonyle puisque ce sont les deux carbones réducteurs des deux monosaccharides qui forment la liaison alpha(1-2) de l'alpha-D-glucose et du bêta-D-fructose. Il est communément appelé sucre, saccharose ou sucrose, ou par les noms chimiques suivants : bêta-D-fructofuranosyl-alpha-D-glucopyranoside (nom IUPAC), alpha-D-glucopyranosyl-bêta-D-fructofuranoside, α-D-glucopyranosyl-(1→2)-β-D-fructofuranoside ; β-D-fructofuranosyl-(2→1)-α-D-glucopyranoside ; β-(2S,3S,4S,4S,5R)-fructofuranosyl-α-(1R,2R,3S,4S,5R)-glucopyranoside ; α-(1R,2R,3S,4S,5R)-glucopyranosyl-β-(2S,3S,4S,5R)-fructofuranoside ; ((2R,3R,4S,5S,5S,6R)-2-[(2S,3S,4S,5R)-3,4-dihydroxy-2,5-bis(hydroxyméthyl)oxapent-2-yl]oxy-6-(hydroxyméthyl)oxahexane-3,4,5-triol). La formule moléculaire du D(+)-sucrose est C12H22O11. Il est obtenu principalement à partir de la canne à sucre et de la betterave sucrière. Le saccharose n'a pas de caractère réducteur car il ne contient aucun atome de carbone anomérique libre, les carbones anomériques sont liés entre eux (les deux groupes OH des carbones carbonyles participent à la liaison O-glycosidique), c'est-à-dire que la liaison glycosidique du saccharose est formée entre les extrémités réductrices du glucose et du fructose, et non entre l'extrémité réductrice de l'un et l'extrémité non réductrice de l'autre. Par conséquent, étant non réducteur, le saccharose est négatif dans le test de Fehling. Le saccharose est optiquement actif. L'activité optique est la propriété d'une substance de faire tourner le plan de la lumière polarisée. Le saccharose fait tourner le plan de polarisation dans le sens des aiguilles d'une montre (sens des aiguilles d'une montre), et est donc appelé un sucre dextrogyre ou dextrogyre (+). La nomenclature D-L fournit une abréviation rapide pour les énantiomères. Ces composés présentent deux formes stéréoisomères et sont désignés par les lettres D- et L- devant le nom du composé, mais ne doivent pas être confondus avec la nomenclature relative à la classification des énantiomères en formes dextrogyre (+) et lévogyre (-), qui fait référence à l'activité optique. Le saccharose, en plus d'être l'édulcorant naturel par excellence de l'alimentation humaine, est le sucre le plus utilisé par l'industrie pharmaceutique pour la production de sirops, de comprimés à mâcher, de dragées, de comprimés, etc. Les sirops contiennent une forte proportion de saccharose, non seulement pour obtenir le goût sucré et la viscosité, mais aussi pour augmenter leur stabilité vis-à-vis des micro-organismes en raison du manque d'eau disponible. Les fortes concentrations de sucre signifient que la pression osmotique élevée du sirop empêche la croissance bactérienne. Le saccharose est également un excipient dans les vaccins. Les vaccins étant des préparations biologiques, ils peuvent être instables une fois créés. Cette instabilité peut réduire la sécurité et l'efficacité du produit biologique ; les vaccins peuvent être sensibles à la chaleur, à la lumière ou aux changements d'environnement. Le saccharose préserve l'efficacité des vaccins en empêchant les molécules de perdre leur forme au cours de leur fabrication, de leur stockage, de leur distribution et, finalement, de leur administration aux patients. Dans l'industrie alimentaire, les sucres servent généralement d'édulcorants, d'exhausteurs de goût, d'antioxydants et de conservateurs. Les réactions chimiques des sucres comprennent les réactions de Maillard ou la formation de composés brunissants et la caramélisation. Le saccharose, en particulier, agit comme un stabilisateur grâce à ses propriétés naturelles de mouillage. Elle est utilisée comme un produit multifonctionnel car elle ne se contente pas de sucrer les aliments, mais aide également les aliments, notamment les produits de boulangerie et de confiserie, à rester frais et à conserver leur humidité ; elle favorise la fermentation du pain et d'autres produits contenant de la levure, améliore le goût et la texture des aliments en général, et est également utilisée comme conservateur et édulcorant dans les jus, les boissons gazeuses, les boissons rafraîchissantes et les boissons alcoolisées. Comme tout autre soluté, l'ajout de sucre à un mélange modifie ses points d'ébullition et de congélation. Par exemple, dans la fabrication de la crème glacée, les sucres réduisent le point de congélation, empêchant l'eau contenue dans la crème glacée de se transformer en glace, ce qui permet d'obtenir une texture lisse et facile à travailler malgré les basses températures. En revanche, pour la production de bonbons, l'augmentation du point d'ébullition est le facteur déterminant pour la texture du produit final. En général, les températures plus élevées (concentration de sucre plus élevée) produisent des caramels plus durs et plus rigides, tandis que les températures plus basses produisent des caramels plus mous. La texture finale d'un bonbon dépend de la concentration en sucre, qui dépend elle-même du point d'ébullition. Pourquoi le saccharose n'a-t-il pas de pouvoir réducteur ?
Le saccharose n'a pas de caractère réducteur car il ne contient pas d'atomes de carbone anomériques libres, les carbones anomériques sont liés entre eux (les deux groupes OH des carbones carbonyles participent à la liaison O-glycosidique), c'est-à-dire que la liaison glycosidique dans le saccharose est formée entre les extrémités réductrices du glucose et du fructose, et non entre l'extrémité réductrice de l'un et l'extrémité non réductrice de l'autre. Par conséquent, n'ayant aucun caractère réducteur, le saccharose est négatif dans le test de Fehling. Le caractère réducteur apparaît dans un disaccharide si l'un des monosaccharides qui le forment a son carbone anomérique (ou carbonyle) libre, c'est-à-dire si ce carbone ne fait pas partie de la liaison O-glycosidique. En d'autres termes, si la liaison O-glycosidique est monocarbonyle, le disaccharide résultant sera réducteur (lactose, maltose), alors que si la liaison O-glycosidique est dicarbonyle, le disaccharide résultant sera non réducteur (saccharose, tréhalose). Le test de Fehling (découvert par le chimiste allemand Hermann von Fehling) est utilisé pour la détection des substances réductrices, notamment les sucres réducteurs. Il est basé sur le pouvoir réducteur du groupe carbonyle d'un aldéhyde qui devient acide en réduisant le sel cuivrique de cuivre (II) dans un milieu alcalin en oxyde de cuivre (I), ce qui forme un précipité rouge. Un aspect important de cette réaction est que la forme aldéhyde peut être facilement détectée, même si elle existe en très petites quantités. Si un sucre réduit le réactif de Fehling en oxyde de cuivre(I) rouge, on dit que c'est un sucre réducteur. Fehling (bleu) + sucre non réducteur = couleur bleue - Fehling (bleu) + sucre réducteur = couleur rouge brique À quoi sert le test de Fehling ?
Le test de Fehling (découvert par le chimiste allemand Hermann von Fehling) est utilisé pour la détection des substances réductrices, notamment les sucres réducteurs. Il est basé sur le pouvoir réducteur du groupe carbonyle d'un aldéhyde qui devient acide en réduisant le sel cuivrique (II) en milieu alcalin en oxyde de cuivre (I), ce qui forme un précipité rouge. Un aspect important de cette réaction est que la forme aldéhyde peut être facilement détectée, même si elle existe en très petites quantités. Si un sucre réduit le réactif de Fehling en oxyde de cuivre(I) rouge, on dit que c'est un sucre réducteur. Fehling (bleu) + sucre non réducteur = couleur bleue ; Fehling (bleu) + sucre réducteur = couleur rouge brique Quelles sont les applications du saccharose ?
Le saccharose, en plus d'être l'édulcorant naturel par excellence de l'alimentation humaine, est le sucre le plus utilisé par l'industrie pharmaceutique pour la production de sirops, de comprimés à mâcher, de dragées, de comprimés, etc. Les sirops contiennent une forte proportion de saccharose, non seulement pour obtenir le goût sucré et la viscosité, mais aussi pour augmenter leur stabilité vis-à-vis des micro-organismes en raison du manque d'eau disponible. Les fortes concentrations de sucre signifient que la pression osmotique élevée du sirop empêche la croissance bactérienne. Le saccharose est également un excipient dans les vaccins. Les vaccins étant des préparations biologiques, ils peuvent être instables une fois créés. Cette instabilité peut réduire la sécurité et l'efficacité du produit biologique ; les vaccins peuvent être sensibles à la chaleur, à la lumière ou aux changements d'environnement. Le saccharose préserve l'efficacité des vaccins en empêchant les molécules de perdre leur forme au cours de leur fabrication, de leur stockage, de leur distribution et, finalement, de leur administration aux patients. Dans l'industrie alimentaire, les sucres servent généralement d'édulcorants, d'exhausteurs de goût, d'antioxydants et de conservateurs. Les réactions chimiques des sucres comprennent les réactions de Maillard ou la formation de composés brunissants et la caramélisation. Le saccharose, en particulier, agit comme un stabilisateur grâce à ses propriétés mouillantes naturelles, est utilisé comme un produit multifonctionnel car il ne se contente pas de sucrer les aliments, mais aide également les aliments, notamment les produits de boulangerie et de pâtisserie, à rester frais et à conserver leur humidité ; il favorise la fermentation du pain et d'autres produits contenant de la levure, améliore le goût et la texture des aliments en général et sert également de conservateur et d'édulcorant dans les jus, les boissons gazeuses, les boissons non alcoolisées et les boissons alcoolisées. Comme tout autre soluté, l'ajout de sucre à un mélange modifie son point d'ébullition et de congélation. Par exemple, dans la fabrication de la crème glacée, les sucres réduisent le point de congélation, empêchant l'eau présente à l'intérieur de la crème glacée de se transformer en glace, ce qui permet d'obtenir une texture lisse et facile à travailler malgré les basses températures. En revanche, pour la production de bonbons, l'augmentation du point d'ébullition est le facteur déterminant pour la texture du produit final. En général, les températures plus élevées (concentration de sucre plus élevée) produisent des caramels plus durs et plus rigides, tandis que les températures plus basses produisent des caramels plus mous. La texture finale d'un bonbon dépend de la concentration en sucre, qui dépend elle-même du point d'ébullition. À quoi sert le D(+)-saccharose ?
Le D(+)-saccharose, ou simplement le saccharose, est le sucre le plus courant. Le D(+)-saccharose, en plus d'être l'édulcorant naturel par excellence de l'alimentation humaine, est le sucre le plus utilisé par l'industrie pharmaceutique pour la production de sirops, de comprimés à mâcher, de dragées, de comprimés, etc. Les sirops contiennent une forte proportion de saccharose, non seulement pour obtenir le goût sucré et la viscosité, mais aussi pour augmenter leur stabilité vis-à-vis des micro-organismes en raison du manque d'eau disponible. Les fortes concentrations de sucre signifient que la pression osmotique élevée du sirop empêche la croissance bactérienne. Le saccharose est également un excipient dans les vaccins. Les vaccins étant des préparations biologiques, ils peuvent être instables une fois créés. Cette instabilité peut réduire la sécurité et l'efficacité du produit biologique ; les vaccins peuvent être sensibles à la chaleur, à la lumière ou aux changements d'environnement. Le saccharose préserve l'efficacité des vaccins en empêchant les molécules de perdre leur forme au cours de leur fabrication, de leur stockage, de leur distribution et, finalement, de leur administration aux patients. Dans l'industrie alimentaire, les sucres servent généralement d'édulcorants, d'exhausteurs de goût, d'antioxydants et de conservateurs. Les réactions chimiques des sucres comprennent les réactions de Maillard ou la formation de composés brunissants et la caramélisation. Le saccharose, en particulier, agit comme un stabilisateur grâce à ses propriétés mouillantes naturelles, est utilisé comme un produit multifonctionnel car il ne se contente pas de sucrer les aliments, mais aide également les aliments, notamment les produits de boulangerie et de pâtisserie, à rester frais et à conserver leur humidité ; il favorise la fermentation du pain et d'autres produits contenant de la levure, améliore le goût et la texture des aliments en général et sert également de conservateur et d'édulcorant dans les jus, les boissons gazeuses, les boissons non alcoolisées et les boissons alcoolisées. Comme tout autre soluté, l'ajout de sucre à un mélange modifie les points d'ébullition et de congélation du mélange. Par exemple, dans la fabrication de la crème glacée, les sucres réduisent le point de congélation, empêchant l'eau contenue dans la crème glacée de se transformer en glace, ce qui permet d'obtenir une texture lisse et facile à travailler malgré les basses températures. En revanche, pour la production de bonbons, l'augmentation du point d'ébullition est le facteur déterminant pour la texture du produit final. En général, les températures plus élevées (concentration de sucre plus élevée) produisent des caramels plus durs et plus rigides, tandis que les températures plus basses produisent des caramels plus mous. La texture finale d'un bonbon dépend de la concentration en sucre, qui dépend elle-même du point d'ébullition. Quel est le rôle du saccharose en tant qu'excipient ?
Le saccharose peut remplir plusieurs fonctions dans l'industrie pharmaceutique, il peut servir de charge ou de diluant, par exemple si la quantité de médicament actif est trop faible pour être manipulée de manière pratique ; de liant pour maintenir ensemble les ingrédients d'une formulation, par exemple dans un comprimé ; de matériau d'enrobage, pour augmenter la viscosité ou également l'une des fonctions clés du saccharose : l'arôme, masquant les goûts désagréables des substances actives et rendant les produits pharmaceutiques plus appétissants. Les concentrations élevées de sucre dans les sirops signifient que la pression osmotique élevée du sirop empêche la croissance bactérienne. Le saccharose est également un excipient dans les vaccins. Le saccharose préserve l'efficacité des vaccins en empêchant les molécules de perdre leur forme au cours de leur fabrication, de leur stockage, de leur distribution et, finalement, de leur administration aux patients. Pourquoi le saccharose est-il appelé D(+)-saccharose ?
Le saccharose est optiquement actif. L'activité optique est la propriété d'une substance de faire tourner le plan de la lumière polarisée. Le saccharose fait tourner le plan de polarisation dans le sens des aiguilles d'une montre (sens des aiguilles d'une montre), il est donc appelé un sucre dextrogyre ou dextrogyre, un isomère optique (+). La nomenclature D-L fournit une abréviation rapide pour les énantiomères. Ces composés présentent deux formes stéréoisomères et sont désignés par les lettres D- et L- devant le nom du composé, mais ne doivent pas être confondus avec la nomenclature relative à la classification des énantiomères en formes dextrogyre (+) et lévogyre (-), qui fait référence à l'activité optique. Les symboles R et S sont actuellement utilisés pour indiquer la configuration, c'est-à-dire la disposition des atomes ou des groupes d'atomes dans l'espace, et dans certains cas, d'autres termes tels que D et L peuvent être utilisés. Que signifie qu'un sucre est réducteur?
Un sucre réducteur est tout sucre capable d'agir comme un agent réducteur. En solution alcaline, un sucre réducteur peut former un aldéhyde ou une cétone, ce qui lui permet d'agir comme agent réducteur, par exemple dans le réactif de Benedict. Dans une telle réaction, le sucre est transformé en acide carboxylique. Tous les monosaccharides sont des sucres réducteurs, de même que certains disaccharides, certains oligosaccharides et certains polysaccharides. Les monosaccharides peuvent être divisés en deux groupes : les aldoses, qui possèdent un groupe aldéhyde, et les cétoses, qui possèdent un groupe cétone. Les cétoses doivent d'abord se tautomériser en aldoses avant de pouvoir jouer le rôle de sucres réducteurs. Les monosaccharides alimentaires courants, le galactose, le glucose et le fructose, sont tous des sucres réducteurs. Les disaccharides sont formés à partir de deux monosaccharides et peuvent être classés comme étant réducteurs ou non réducteurs. Les disaccharides non réducteurs, tels que le saccharose et le tréhalose, ont des liaisons glycosidiques entre leurs carbones anomériques et ne peuvent donc pas être convertis en une forme à chaîne ouverte avec un groupe aldéhyde ; ils sont cycliquement fermés. Les disaccharides réducteurs, comme le lactose et le maltose, n'ont qu'un seul de leurs deux carbones anomériques impliqués dans la liaison glycosidique, tandis que l'autre est libre et peut être converti en une forme à chaîne ouverte avec un groupe aldéhyde. Le groupe fonctionnel aldéhyde permet au sucre d'agir comme un agent réducteur, par exemple dans le test de Tollens ou le test de Benedict. Les formes hémiacétales cycliques des aldoses peuvent être ouvertes pour révéler un aldéhyde, et certains cétoses peuvent subir une tautomérisation pour devenir des aldoses. Cependant, les acétals, y compris ceux que l'on trouve dans les liaisons polysaccharides, ne peuvent pas être facilement convertis en aldéhydes libres. Les sucres réducteurs réagissent avec les acides aminés dans la réaction de Maillard, une série de réactions qui se produisent lorsque les aliments sont cuits à haute température et qui jouent un rôle important dans la détermination du goût des aliments. En outre, les niveaux de sucres réducteurs dans le vin, le jus et la canne à sucre sont indicatifs de la qualité de ces produits alimentaires. Quel est le point de fusion du saccharose?
Aucun. Le saccharose se décompose à 186 °C. Il ne fond pas, mais lorsqu'il atteint la température de décomposition, le saccharose se décompose en fructose et en glucose. Le chauffage du saccharose implique un processus thermique complexe comprenant à la fois la fusion et la décomposition. En fonction de la vitesse à laquelle il est chauffé, on observera différentes choses. En fait, le saccharose commence à se décomposer lorsqu'il commence à fondre. Si de l'eau est présente pendant le processus de chauffage, une réaction connue sous le nom d'inversion du saccharose se produit et le saccharose se décompose en ses composants, une molécule de glucose et une molécule de fructose. Cependant, si le saccharose sec est chauffé jusqu'à son point de fusion ou de décomposition, des choses plus complexes se produisent. Des quantités significatives de glucose sont initialement détectées. La poursuite du chauffage conduit à la "caramélisation". La caramélisation est un processus de condensation au cours duquel l'eau est retirée du saccharose ; la perte d'eau initiale est suivie d'une isomérisation et d'une polymérisation. Pendant la caramélisation, plusieurs milliers de composés différents se formeraient. Des études sont toujours en cours pour tenter de les identifier tous. Lorsque ce mélange complexe refroidit, ce n'est plus du saccharose. Quelle est la solubilité du saccharose?
La solubilité du saccharose dans l'eau est de 2039 g/L à 20 °C. Que désigne l'expression sucre inverti ?
Le sucre inverti est un sirop composé de glucose et de fructose (monosaccharides) obtenu par hydrolyse du saccharose (disaccharide). L'hydrolyse du saccharose génère un mélange équimolaire de fructose et de glucose, commercialement connu sous le nom de sucre inverti, appelé ainsi en raison du changement de rotation qui modifie ses propriétés optiques, passant d'une rotation positive ou dextrogyre à une rotation négative ou lévogyre. Le saccharose est dextrogyre, avec une rotation spécifique de +66,5° ; lorsqu'il est clivé en glucose (ou dextrose) qui est dextrogyre, avec une rotation spécifique de [α] D = +52,7° et en fructose (lévulose) fortement lévogyre, avec une rotation spécifique de [α] D = -92°, le mélange résultant est lévogyre, c'est-à-dire que le sens de rotation du plan de vibration de la lumière a été inversé par rapport au saccharose d'origine, d'où le nom de sucre inversé. L'inversion du saccharose peut être réalisée par hydrolyse acide, ou par hydrolyse enzymatique (à l'aide d'invertase). Le sucre inverti peut également être appelé : sirop inverti, sirop de sucre inverti, sirop simple, sirop de sucre, sirop USP, saccharose inverti, eau sucrée ou sirop de barre. Le sirop de sucre inverti est 30% plus sucré que le saccharose et plus facile à incorporer dans les préparations alimentaires et pharmaceutiques, car il ne présente pas les problèmes de cristallisation de son précurseur (le saccharose), qui cristallise dans les solutions très concentrées. Quelle est la rotation spécifique du D(+)-sucrose?
La rotation spécifique du D-(+)-sucrose α 20/D c=26 (dans H2O) est de +66,5°. En général, la rotation diminue linéairement avec l'augmentation de la température ; cependant, la différence entre la rotation observée à 20 et 25 °C est généralement négligeable. Généralement, dans les pharmacopées, les mesures sont effectuées à 25 °C, en utilisant la ligne D du sodium à la longueur d'onde de 589 nm. La rotation spécifique ainsi déterminée est exprimée par α 25/D. Comment mesure-t-on la rotation spécifique du saccharose ?
La rotation spécifique ([α]) est une propriété d'un composé chimique chiral. Elle est définie comme le changement d'orientation de la lumière monochromatique polarisée dans le plan, par unité de produit distance-concentration, lorsque la lumière traverse un échantillon d'un composé en solution. Les composés qui font tourner le plan de polarisation d'un faisceau lumineux polarisé dans le sens des aiguilles d'une montre sont dits dextrogyres, ce qui correspond à des valeurs positives de rotation spécifique, tandis que les composés qui font tourner le plan de polarisation de la lumière polarisée dans le sens inverse des aiguilles d'une montre sont dits lévogyres, ce qui correspond à des valeurs négatives. Si un composé est capable de faire tourner le plan de polarisation de la lumière polarisée plane, on dit qu'il est "optiquement actif". La polarimétrie est une technique qui permet de distinguer les isomères optiquement actifs les uns des autres en mesurant la rotation optique d'une substance ; elle constitue également un critère important d'identité et de pureté et peut être utilisée à des fins quantitatives. Quel est le numéro CAS du saccharose ?
Le numéro CAS du saccharose est 57-50-1. Qu'est-ce que le numéro CAS 57-50-1 ?
Le numéro CAS 57-50-1 correspond au D(+)-saccharose. Il est communément appelé sucre, saccharose ou sucrose, ou par les noms chimiques suivants : bêta-D-fructofuranosyl-alpha-D-glucopyranoside (nom IUPAC), alpha-D-glucopyranosyl-bêta-D-fructofuranoside, α-D-glucopyranosyl-(1→2)-β-D-fructofuranoside ; β-D-fructofuranosyl-(2→1)-α-D-glucopyranoside ; β-(2S,3S,4S,5R)-fructofuranosyl-α-(1R,2R,3S,4S,5R)-glucopyranoside ; α-(1R,2R,3S,3S,4S,5R)-glucopyranosyl-β-(2S,3S,4S,5R)-fructofuranoside ; ((2R,3R,4S,5S,5S,6R)-2-[(2S,3S,4S,5R)-3,4-dihydroxy-2,5-bis(hydroxyméthyl)oxapent-2-yl]oxy-6-(hydroxyméthyl)oxahexane-3,4,5-triol) Que sont les degrés Brix ?
La mesure du Brix est une application bien connue dans l'industrie alimentaire et des boissons, entre autres. Au sens strict, la mesure du Brix consiste à déterminer la teneur en saccharose pur dans l'eau : 1 degré Brix (°Bx) = 1 g de saccharose / dans 100 g de solution Dans le cas des fruits et légumes, cette valeur indique la quantité de sucre (saccharose) présente, ce qui a une influence déterminante sur leur goût. La mesure de la quantité de sucre dans les fruits frais est essentielle pour connaître leur état de maturité et le moment optimal de leur récolte, en fonction du type de produit et de sa variété spécifique. Il existe des réglementations nationales et internationales en matière de qualité qui établissent des degrés Brix minimums pour la commercialisation adéquate de chaque produit". Comment mesure-t-on les degrés Brix ?
Différents instruments peuvent être utilisés pour mesurer les degrés Brix, bien que le plus courant soit le réfractomètre. Un réfractomètre détermine le Brix en mesurant la réfraction de la lumière traversant un échantillon de liquide. Les liquides contenant des sucres et/ou d'autres solides dissous sont plus denses que l'eau et provoquent une plus grande réfraction lors du passage de la lumière. L'instrument compare ce résultat avec la réfraction de la lumière dans l'eau et donne une valeur Brix. L'indice de réfraction dépend non seulement de la longueur d'onde utilisée pour la mesure, mais aussi de la température de la solution mesurée. Il existe une relation directe entre l'indice de réfraction et la valeur Brix. L'indice de réfraction mesuré est directement converti en teneur en solides en poids (°Brix). L'échelle de Brix est une échelle populaire dérivée de l'indice de réfraction d'une solution à 20 °C. Où acheter du saccharose
Vous pouvez acheter du saccharose auprès d'ITW Reagents par le biais de son réseau mondial de distributeurs, ou sur la boutique en ligne si vous êtes un client enregistré d'ITW Reagents. Si vous souhaitez acheter du saccharose pour les processus de production, veuillez consulter nos distributeurs. Suivez ce lien pour trouver un distributeur dans votre pays https://itwreagents.com/rest-of-world/es/distribuidores-rw.